La polmonite nosocomiale è l'infezione nosocomiale più comune e grave, di cui la polmonite associata alla ventilazione (VAP) rappresenta il 40%. La VAP causata da patogeni refrattari rappresenta ancora un problema clinico complesso. Per anni, le linee guida hanno raccomandato una serie di interventi (come la sedazione mirata e l'elevazione della testa) per prevenire la VAP, ma la VAP si verifica fino al 40% dei pazienti sottoposti a intubazione tracheale, con conseguenti degenze ospedaliere più lunghe, aumento dell'uso di antibiotici e decesso. Le persone sono sempre alla ricerca di misure preventive più efficaci.
La polmonite associata alla ventilazione (VAP) è una polmonite di nuova insorgenza che si sviluppa 48 ore dopo l'intubazione tracheale ed è l'infezione nosocomiale più comune e mortale in terapia intensiva (UTI). Le linee guida del 2016 dell'American Society of Infectious Diseases hanno distinto la VAP dalla definizione di polmonite acquisita in ospedale (HAP) (HAP si riferisce solo alla polmonite che si verifica dopo il ricovero ospedaliero senza tubo tracheale e non è correlata alla ventilazione meccanica; VAP è la polmonite dopo intubazione tracheale e ventilazione meccanica), e la Società Europea e la Cina ritengono che la VAP sia ancora un tipo speciale di HAP [1-3].
Nei pazienti sottoposti a ventilazione meccanica, l'incidenza della VAP varia dal 9% al 27%, il tasso di mortalità è stimato al 13% e può portare a un aumento dell'uso di antibiotici sistemici, ventilazione meccanica prolungata, degenza prolungata in terapia intensiva e aumento dei costi [4-6]. La HAP/VAP nei pazienti non immunodeficienti è solitamente causata da un'infezione batterica e la distribuzione dei patogeni comuni e le loro caratteristiche di resistenza variano a seconda della regione, della classe ospedaliera, della popolazione di pazienti e dell'esposizione agli antibiotici e cambiano nel tempo. Pseudomonas aeruginosa ha dominato i patogeni correlati alla VAP in Europa e America, mentre Acinetobacter baumannii è stato isolato in misura maggiore negli ospedali terziari in Cina. Da un terzo alla metà di tutti i decessi correlati alla VAP sono causati direttamente dall'infezione, con un tasso di mortalità dei casi causati da Pseudomonas aeruginosa e acinetobacter più elevato [7,8].
A causa della forte eterogeneità della VAP, la specificità diagnostica delle sue manifestazioni cliniche, delle immagini diagnostiche e dei test di laboratorio è bassa e il range di diagnosi differenziale è ampio, il che rende difficile diagnosticare la VAP in tempo. Allo stesso tempo, la resistenza batterica rappresenta una seria sfida per il trattamento della VAP. Si stima che il rischio di sviluppare VAP sia del 3%/giorno durante i primi 5 giorni di utilizzo della ventilazione meccanica, del 2%/giorno tra 5 e 10 giorni e dell'1%/giorno per il resto del tempo. Il picco di incidenza si verifica generalmente dopo 7 giorni di ventilazione, quindi esiste una finestra temporale in cui l'infezione può essere prevenuta precocemente [9,10]. Molti studi hanno esaminato la prevenzione della VAP, ma nonostante decenni di ricerca e tentativi di prevenirla (come evitare l'intubazione, prevenire la reintubazione, ridurre la sedazione, sollevare la testa del letto da 30° a 45° e l'igiene orale), l'incidenza non sembra essere diminuita e il carico medico associato rimane molto elevato.
Gli antibiotici per via inalatoria sono stati utilizzati per trattare le infezioni croniche delle vie aeree fin dagli anni '40. Poiché possono massimizzare la distribuzione dei farmaci al sito bersaglio dell'infezione (ovvero le vie aeree) e ridurre gli effetti collaterali sistemici, hanno dimostrato un buon valore applicativo in una varietà di patologie. Gli antibiotici per via inalatoria sono ora approvati dalla Food and Drug Administration (FDA) statunitense e dall'Agenzia europea per i medicinali (EMA) per l'uso nella fibrosi cistica. Gli antibiotici per via inalatoria possono ridurre significativamente la carica batterica e la frequenza delle riacutizzazioni nelle bronchiectasie senza aumentare gli eventi avversi complessivi, e le attuali linee guida li hanno riconosciuti come trattamento di prima linea per i pazienti con infezione da Pseudomonas aeruginosa e riacutizzazioni frequenti; gli antibiotici per via inalatoria durante il periodo perioperatorio del trapianto polmonare possono anche essere utilizzati come farmaci adiuvanti o profilattici [11,12]. Tuttavia, nelle linee guida statunitensi del 2016 sulla VAP, gli esperti non avevano fiducia nell'efficacia degli antibiotici per via inalatoria adiuvanti a causa della mancanza di ampi studi clinici randomizzati controllati. Anche lo studio di fase 3 (INHALE) pubblicato nel 2020 non è riuscito a ottenere risultati positivi (inalazione di antibiotici per via endovenosa assistita da amikacina per infezioni batteriche Gram-negative causate da pazienti con polmonite associata alla ventilazione (VAP), uno studio di fase 3 sull'efficacia, in doppio cieco, randomizzato, controllato con placebo, su un totale di 807 pazienti, farmaco sistemico + inalazione assistita di amikacina per 10 giorni).
In questo contesto, un team guidato da ricercatori del Centro Ospedaliero Universitario Regionale di Tours (CHRU) in Francia ha adottato una strategia di ricerca diversa e ha condotto uno studio di efficacia randomizzato, controllato, in doppio cieco, multicentrico e avviato da un ricercatore (AMIKINHAL). L'amikacina inalata o il placebo per la prevenzione della VAP sono stati confrontati in 19 unità di terapia intensiva in Francia [13].
Un totale di 847 pazienti adulti sottoposti a ventilazione meccanica invasiva tra le 72 e le 96 ore sono stati assegnati in modo casuale, in rapporto 1:1, all'inalazione di amikacina (N= 417,20 mg/kg di peso corporeo ideale, QD) o all'inalazione di placebo (N=430, equivalente allo 0,9% di cloruro di sodio) per 3 giorni. L'endpoint primario era il primo episodio di VAP dall'inizio dell'assegnazione randomizzata al giorno 28.
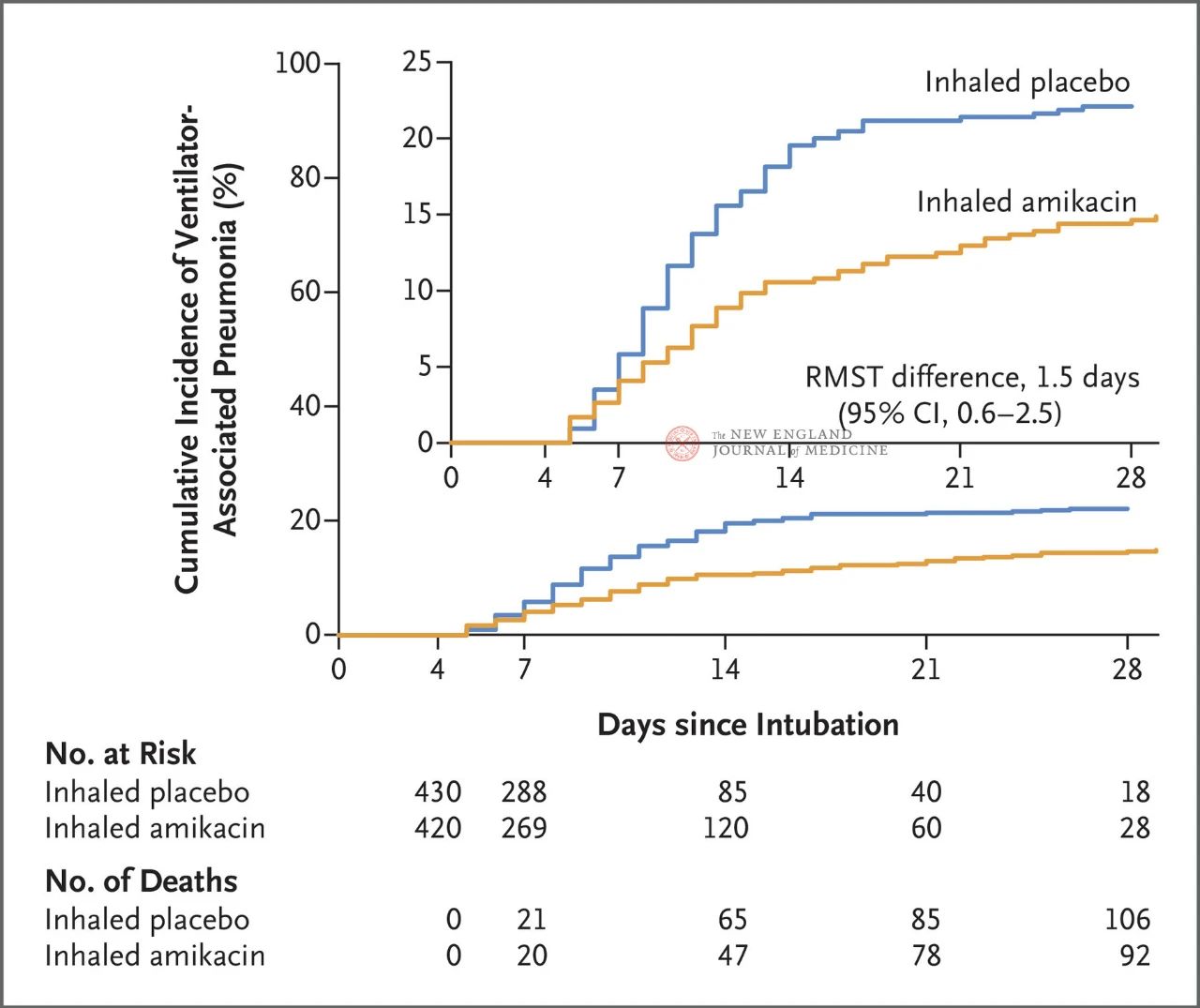
I risultati dello studio hanno mostrato che a 28 giorni, 62 pazienti (15%) nel gruppo trattato con amikacina avevano sviluppato VAP e 95 pazienti (22%) nel gruppo trattato con placebo avevano sviluppato VAP (la differenza media limitata di sopravvivenza per VAP era di 1,5 giorni; IC al 95%, 0,6~2,5; P=0,004).
In termini di sicurezza, sette pazienti (1,7%) nel gruppo amikacina e quattro pazienti (0,9%) nel gruppo placebo hanno manifestato eventi avversi gravi correlati allo studio. Tra coloro che non presentavano danno renale acuto al momento della randomizzazione, 11 pazienti (4%) nel gruppo amikacina e 24 pazienti (8%) nel gruppo placebo hanno manifestato danno renale acuto al giorno 28 (HR, 0,47; IC al 95%, 0,23~0,96).
Lo studio clinico ha presentato tre punti salienti. In primo luogo, in termini di disegno dello studio, lo studio AMIKINHAL si basa sullo studio IASIS (uno studio di fase 2 parallelo, randomizzato, in doppio cieco, controllato con placebo, che ha coinvolto 143 pazienti). Per valutare la sicurezza e l'efficacia dell'inalazione di amikacina e fosfomicina (trattamento sistemico delle infezioni batteriche Gram-negative causate da VAP), e lo studio INHALE, che si è concluso con risultati negativi, ha tratto spunto dalle lezioni apprese, incentrate sulla prevenzione della VAP, ottenendo risultati relativamente buoni. A causa delle caratteristiche di elevata mortalità e lunga degenza ospedaliera nei pazienti sottoposti a ventilazione meccanica e VAP, se l'inalazione di amikacina potesse ottenere risultati significativamente diversi nel ridurre la mortalità e la degenza ospedaliera in questi pazienti, sarebbe più utile per la pratica clinica. Tuttavia, data l'eterogeneità del trattamento e delle cure tardive in ciascun paziente e in ciascun centro, diversi fattori confondenti possono interferire con lo studio, quindi potrebbe essere difficile ottenere un risultato positivo attribuibile agli antibiotici inalatori. Pertanto, uno studio clinico di successo richiede non solo un'eccellente progettazione dello studio, ma anche la selezione di endpoint primari appropriati.
In secondo luogo, sebbene gli antibiotici aminoglicosidici non siano raccomandati come singolo farmaco in varie linee guida sulla VAP, possono coprire i patogeni comuni nei pazienti con VAP (tra cui Pseudomonas aeruginosa, Acinetobacter, ecc.) e, grazie al loro limitato assorbimento nelle cellule epiteliali polmonari, all'elevata concentrazione nel sito di infezione e alla bassa tossicità sistemica, gli antibiotici aminoglicosidici sono ampiamente preferiti tra gli antibiotici per via inalatoria. Questo articolo è coerente con la stima completa dell'entità dell'effetto della somministrazione intratracheale di gentamicina in piccoli campioni pubblicata in precedenza, che dimostra congiuntamente l'effetto degli antibiotici aminoglicosidici per via inalatoria nella prevenzione della VAP. Va inoltre notato che la maggior parte dei controlli placebo selezionati negli studi relativi agli antibiotici per via inalatoria è costituita da soluzione salina normale. Tuttavia, considerando che l'inalazione atomizzata di soluzione fisiologica può svolgere un certo ruolo nella diluizione dell'espettorato e nell'effetto espettorante, la soluzione fisiologica può causare una certa interferenza nell'analisi dei risultati dello studio, che dovrebbe essere presa in considerazione in modo esauriente nello studio.
Inoltre, l'adattamento locale della terapia farmacologica per HAP/VAP è importante, così come la profilassi antibiotica. Allo stesso tempo, indipendentemente dalla durata dell'intubazione, l'ecologia della terapia intensiva locale rappresenta il fattore di rischio più importante per le infezioni da batteri multiresistenti. Pertanto, il trattamento empirico dovrebbe basarsi il più possibile sui dati microbiologici degli ospedali locali e non può basarsi ciecamente sulle linee guida o sull'esperienza degli ospedali terziari. Allo stesso tempo, i pazienti critici che necessitano di ventilazione meccanica sono spesso associati a malattie multisistemiche e, sotto l'azione combinata di molteplici fattori come lo stress, può verificarsi anche un fenomeno di contaminazione microbica intestinale con i polmoni. L'elevata eterogeneità delle patologie causata dalla sovrapposizione interna ed esterna determina inoltre che la promozione clinica su larga scala di ogni nuovo intervento è ancora lontana.
Data di pubblicazione: 02-12-2023