L'iperlipidemia mista è caratterizzata da livelli plasmatici elevati di lipoproteine a bassa densità (LDL) e lipoproteine ricche di trigliceridi, che comportano un aumento del rischio di malattie cardiovascolari aterosclerotiche in questa popolazione di pazienti.
L'ANGPTL3 inibisce la lipoproteina lipasi e l'endosepiasi, nonché l'assorbimento epatico delle lipoproteine ricche di trigliceridi. I portatori della variante inattivata di ANGPTL3 presentavano livelli più bassi di trigliceridi, colesterolo LDL, colesterolo delle lipoproteine ad alta densità (HDL) e colesterolo non-HDL, nonché un minor rischio di malattie cardiovascolari aterosclerotiche. Zodasiran è un farmaco a base di piccoli RNA interferenti (RNAi) che agisce sull'espressione di ANGPTL3 nel fegato.
L'iperlipidemia mista si riferisce a livelli elevati di colesterolo legato alle lipoproteine a bassa densità (LDL-C) e lipoproteine ricche di trigliceridi. Le lipoproteine ricche di trigliceridi (inclusi chilomicroni, lipoproteine a bassissima densità (VLDL) e colesterolo residuo) svolgono un ruolo importante nello sviluppo della malattia aterosclerotica. Non esiste un trattamento efficace per l'iperlipidemia mista.
È noto che il Bates riduce i livelli di trigliceridi (TG), ma la riduzione è limitata. Allo stesso tempo, i farmaci ipolipemizzanti, incluso il Bates (come l'acido acetico eicosapentaenoico, ecc.), non hanno un effetto significativo sul rischio di malattia aterosclerotica causata da elevati livelli di colesterolo residuo. Inoltre, studi precedenti su pazienti già in trattamento con statine hanno dimostrato che la combinazione di farmaci ipolipemizzanti non riduce il rischio di eventi cardiovascolari. Questi fattori rendono molto difficile il trattamento dell'iperlipidemia mista.
L'ANGPTL3 (proteina 3 simile all'angiopoietina) regola il metabolismo dei lipidi e delle lipoproteine, inclusi i trigliceridi e il colesterolo non-HDL (colesterolo-HDL), inibendo reversibilmente la lipoproteina lipasi, l'endosepiasi e l'assorbimento epatico delle lipoproteine dipendente dal recettore delle lipoproteine a bassa densità (LDL). È stato scoperto che la variante di inattivazione dell'ANGPTL3 porta a un aumento dell'attività della lipoproteina lipasi e dell'endosepiasi, che a sua volta porta a bassi livelli plasmatici di lipoproteine nella maggior parte dei casi. Queste includono lipoproteine ricche di trigliceridi (ad esempio chilomicroni, colesterolo residuo, VLDL, lipoproteine a media densità [IDL]), LDL, lipoproteine ad alta densità (HDL), lipoproteine (a) e i loro componenti di colesterolo. Le persone eterozigoti portatrici di questa variante hanno un rischio ridotto di circa il 40% di malattia aterosclerotica e non è stato riscontrato alcun fenotipo clinico avverso. L'ANGPTL3 è espresso nel fegato e le terapie di silenziamento genico che prendono di mira il suo mRNA, note come farmaci a piccolo RNA interferente (siRNA), rappresentano un promettente trattamento ibrido per l'iperlipidemia.
Il 12 settembre 2024, il New England Journal of Medicine (NEJM) ha pubblicato uno studio ARCHES 2 che conferma che il farmaco siRNA zodasiran ha ridotto significativamente i livelli di TG in pazienti con iperlipidemia mista [1]. ARCHES-2 è uno studio di fase 2b, in doppio cieco, controllato con placebo, di esplorazione dell'intervallo di dose. Sono stati arruolati un totale di 204 pazienti con iperlipidemia mista (livelli di TG a digiuno 150-499 mg/dL, livelli di LDL-C ≥70 mg/dL o livelli di non-HDL-C ≥100 mg/dL). I pazienti sono stati suddivisi in gruppi trattati con zodasiran 50 mg, 100 mg, 200 mg e gruppo di controllo placebo. I pazienti hanno ricevuto iniezioni sottocutanee alla settimana 1 e 12 e hanno ricevuto una profilassi di follow-up fino alla settimana 36.
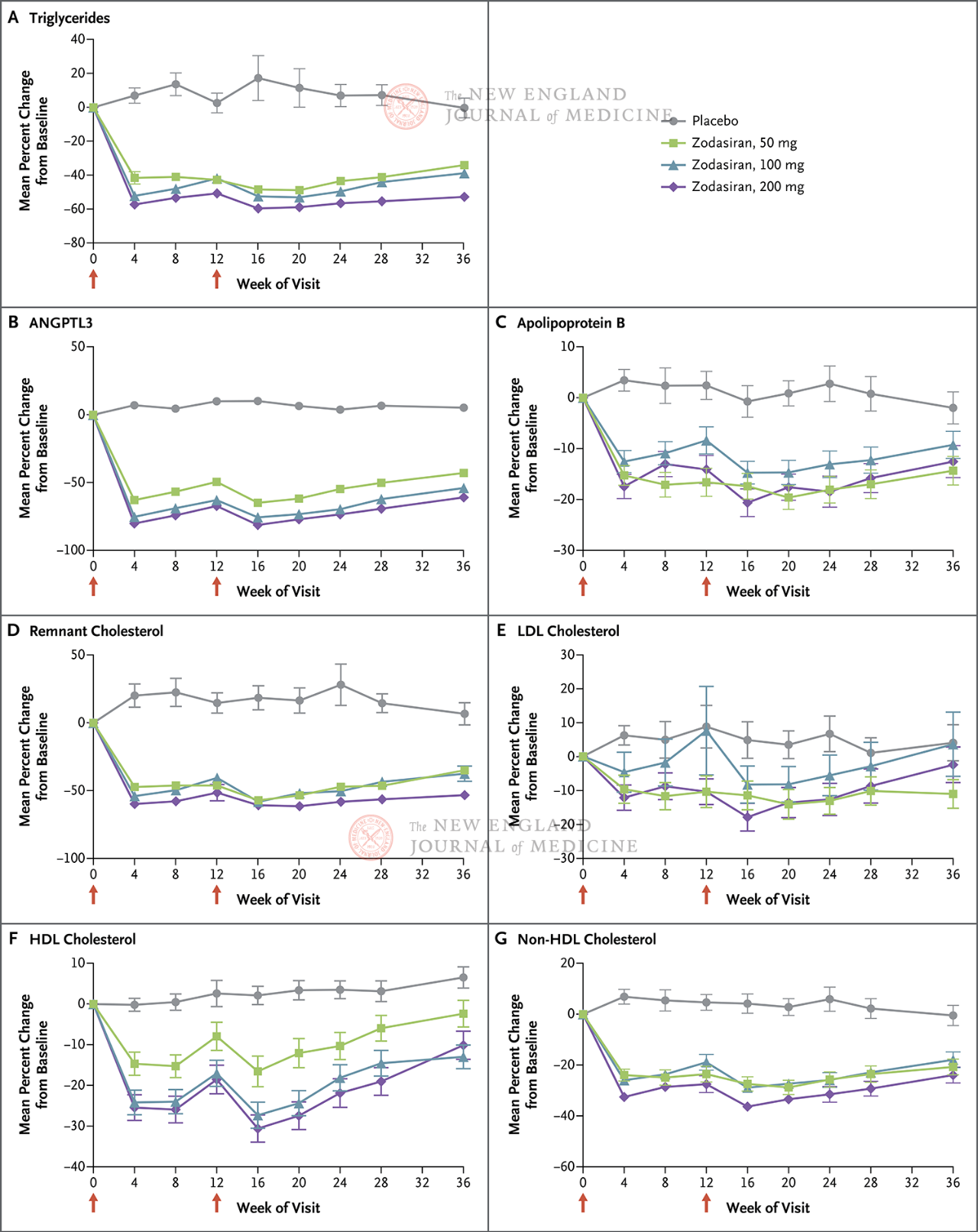
L'endpoint primario era la variazione percentuale dei TG dal basale alla settimana 24. Lo studio ha rilevato che entro la settimana 24, i livelli di TG nel gruppo zodasiran si sono ridotti significativamente in modo dose-dipendente (i livelli di TG in ciascun gruppo di dosaggio si sono ridotti rispettivamente di 51, 57 e 63 punti percentuali, rispetto a quelli del gruppo placebo) (P < 0,001 per tutti i confronti). Anche l'ANGPTL3 è diminuito rispettivamente di 54 punti percentuali, 70 punti percentuali e 74 punti percentuali. I livelli di colesterolo non-HDL sono diminuiti rispettivamente di 29 punti percentuali, 29 punti percentuali e 36 punti percentuali, i livelli di apolipoproteina B sono diminuiti rispettivamente di 19 punti percentuali, 15 punti percentuali e 22 punti percentuali e i livelli di colesterolo LDL sono diminuiti rispettivamente di 16 punti percentuali, 14 punti percentuali e 20 punti percentuali, e questi risultati sono persistiti fino alla 36a settimana. Nella settimana 24, zodasiran
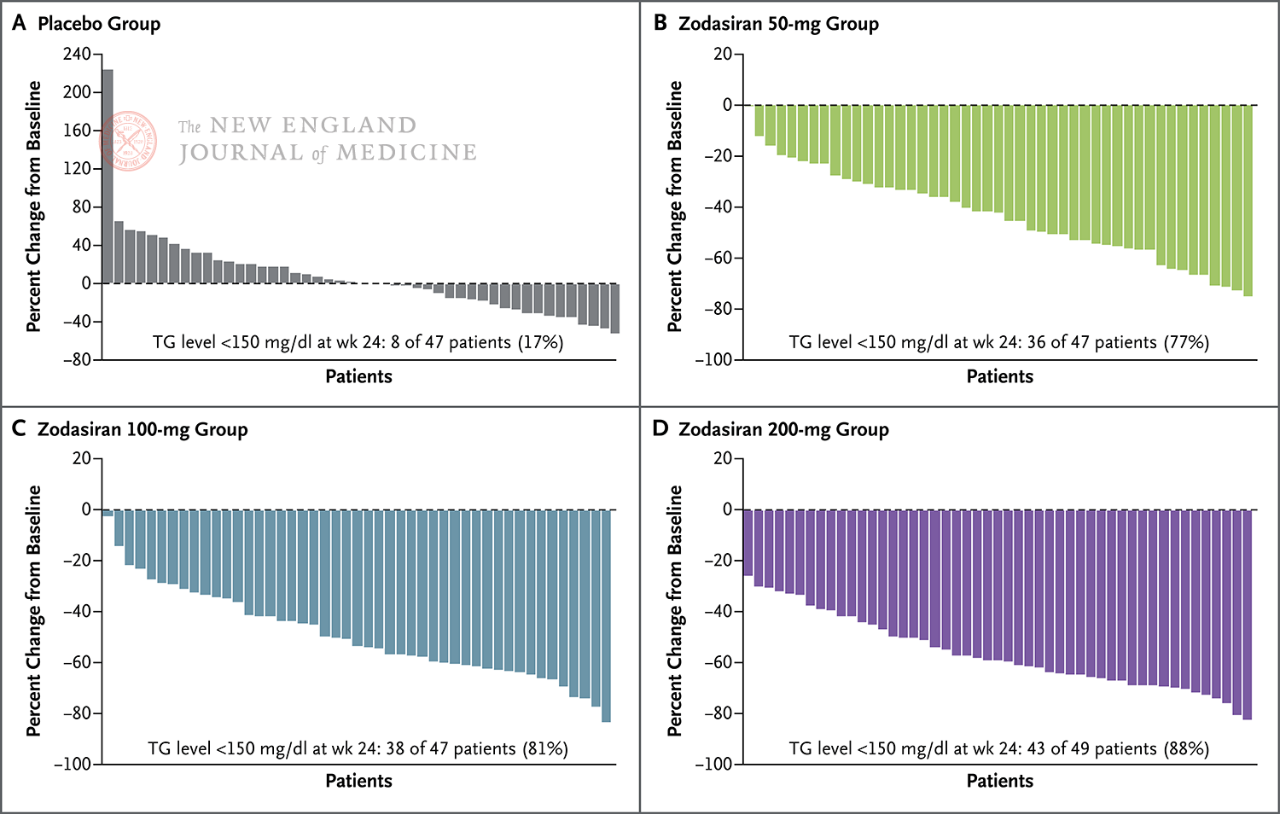
Nell'88% dei pazienti del gruppo trattato con 200 mg, i TG a digiuno erano scesi nella norma.
Le frecce rosse nei giorni 1 e 12 indicano la somministrazione di zodasiran o placebo.
I livelli di TG a digiuno sono diminuiti fino a raggiungere la normalità alla settimana 24 (150
mg/dL o meno)
Ogni pilastro rappresenta un paziente.
Lo studio ha inoltre osservato che zotasiran era sicuro in tutti i gruppi di dosaggio, con solo 2 pazienti che hanno interrotto lo studio a causa di eventi avversi (1 nel gruppo placebo e 1 nel gruppo zotasiran 100 mg). Tutti gli eventi avversi gravi nel gruppo zotasiran si sono risolti entro la fine dello studio e si è verificato un decesso nel gruppo placebo. L'unico evento avverso preoccupante è stato un aumento dell'HBA1c nel gruppo zotasiran 200 mg rispetto al placebo (variazione media dal basale alla settimana 24 [±DS], 0,38±0,66% vs. -0,03±0,88% nei pazienti con diabete preesistente). Nei pazienti senza diabete, la percentuale era dello 0,12±0,19% vs. -0,03±0,19%).
In particolare, quasi tutti i pazienti dello studio (96%) erano trattati con statine (il 37% delle quali ad alto dosaggio), l'1% era trattato con un inibitore dell'enzima di conversione delle proproteine subtilisina 9 (PCSK9i) e il 21% era trattato con fibrati. Pertanto, l'aggiunta di zodasiran sulla base dell'attuale regime terapeutico convenzionale ha comunque ottenuto notevoli effetti ipolipemizzanti, il che rappresenta un nuovo regime per il trattamento futuro dell'iperlipidemia mista.
Alla settimana 24, la dose massima di 200 mg di zotasiran nello studio ha ridotto i livelli di colesterolo residuo di 34,4 mg/dL rispetto al placebo. Sulla base dei modelli attuali, si prevede che questa riduzione ridurrà gli eventi avversi cardiaci maggiori del 20%. Zodasiran ha il potenziale per essere utilizzato come monoterapia per tutti i componenti lipoproteici al fine di ridurre il rischio di eventi cardiovascolari nei pazienti. Sono pertanto necessarie ulteriori ricerche per determinare il potenziale di questo farmaco nel ridurre il rischio di malattia aterosclerotica.
Lo studio MUIR di fase 2b, in doppio cieco, randomizzato, controllato con placebo, pubblicato contemporaneamente su NEJM, ha utilizzato un altro farmaco a base di siRNA, plozasiran, per trattare l'iperlipidemia mista [2]. plozasiran è progettato per ridurre l'espressione di APOC3, il gene che codifica l'apolipoproteina C3 (APOC3), un regolatore del metabolismo dei TG, nel fegato, riducendo così i livelli di TG e di colesterolo residuo. Le riduzioni dei livelli di TG e di colesterolo residuo osservate nello studio erano simili a quelle riscontrate nello studio ARCHES-2. Pertanto, si ipotizza che nei pazienti con iperlipidemia mista, i due farmaci abbiano effetti simili nel ridurre i livelli di lipoproteine ricche di trigliceridi e di colesterolo residuo.
I risultati dei due studi sugli siRNA dimostrano che si tratta di una classe di farmaci molto promettente che offrirà nuove opzioni per il trattamento dell'iperlipidemia mista e migliorerà i risultati cardiovascolari nei pazienti.
Data di pubblicazione: 15-09-2024